Sur la base des premiers « robots vivants à cellules de grenouille » (xénobots), l'équipe de recherche scientifique de l'Institut Wyss de l'Université Tufts et de l'Université Harvard a repoussé une fois de plus les limites de la bio-ingénierie et a créé une nouvelle machine vivante miniature dotée de son propre système nerveux : les « neurobots ». Il a démontré des réseaux neuronaux auto-organisés et des modèles comportementaux plus complexes, ouvrant ainsi une nouvelle fenêtre pour comprendre comment les organismes construisent des structures fonctionnelles.
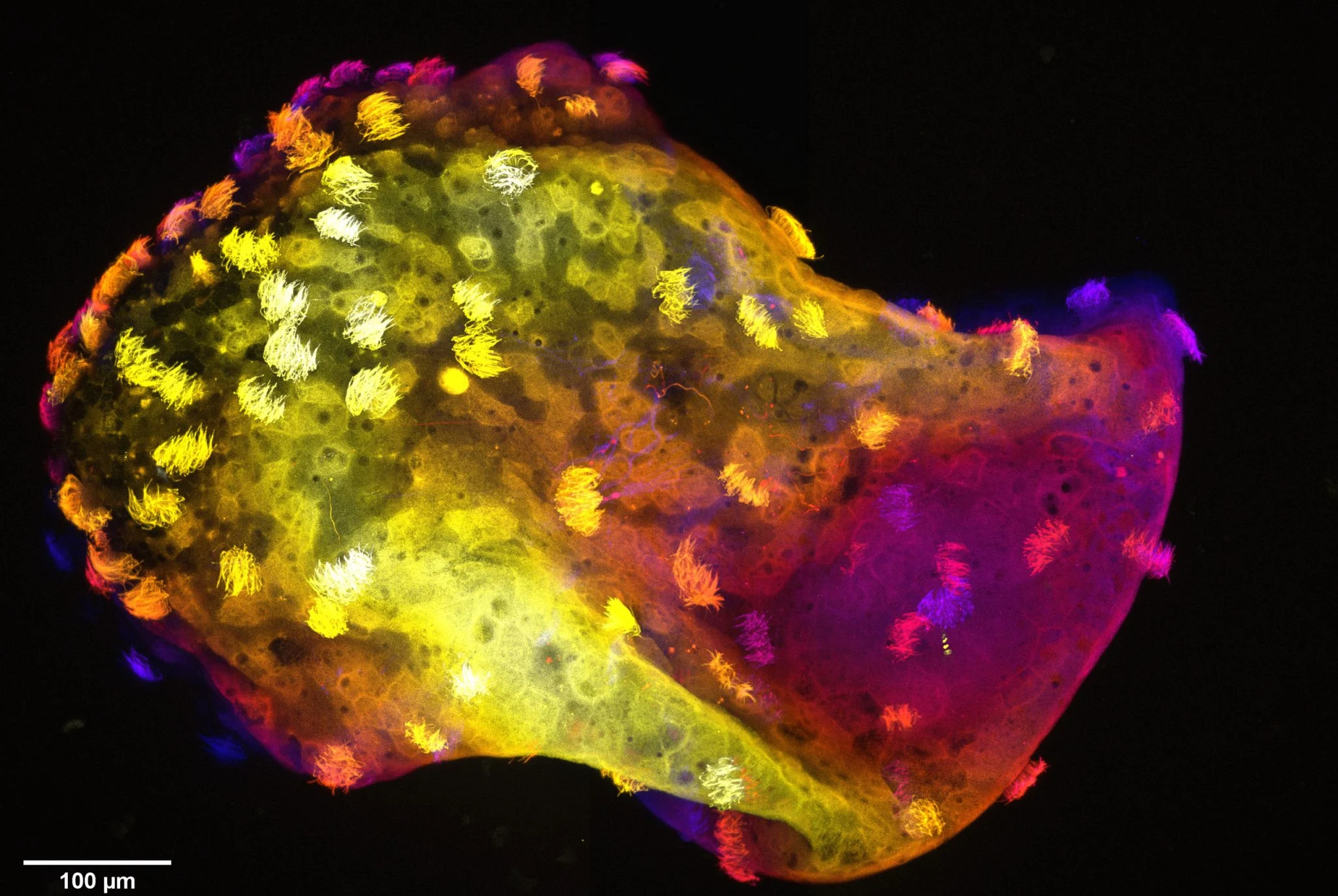
Dès 2020, des chercheurs de l’Université Tufts ont utilisé des cellules embryonnaires de Xenopus laevis pour construire des structures biologiques « de type robot » à l’échelle micronique – des robots à cellules de grenouille. Ils peuvent se déplacer dans l’eau, se réparer et même rassembler des cellules dispersées pour générer de nouveaux individus. Les structures, qui s'auto-assemblent entièrement à partir de cellules vivantes sans échafaudage ni modification génétique, vivent environ 9 à 10 jours et dépendent des nutriments stockés dans les cellules embryonnaires d'origine pour survivre. Sur cette base, l'équipe de recherche a exploré : que se passerait-il si ces structures vivantes étaient « équipées » de systèmes nerveux ?
Dans les dernières recherches, les scientifiques ont implanté un groupe de cellules précurseurs neurales qui se transformeront en neurones dans un robot biologique en construction pour former ce qu'on appelle un « neurobot ». Ces cellules sont intégrées dans la courte fenêtre de temps où le tissu sphérique en est encore aux premiers stades de développement, puis mûrissent progressivement, développent des dendrites et des axones, et s'étendent vers l'intérieur et la surface pour construire un réseau neuronal simple et complet. Des résultats pertinents ont été récemment publiés dans la revue Advanced Science.
Le projet, codirigé par Michael Levin, professeur Vannevar Bush de biologie à l'Université Tufts, et Haleh Fotowat du Wyss Institute, fait partie d'un effort de recherche plus vaste visant à comprendre comment des groupes de cellules s'auto-organisent en structures complexes dans des environnements inconnus. Les chercheurs espèrent que ce type de système « à partir de zéro » pourra révéler les règles de base de la formation et du façonnage du système nerveux, fournissant ainsi une base théorique pour la biologie synthétique et la médecine régénérative, qui pourraient être utilisées pour concevoir de nouvelles structures biologiques ou réparer des tissus endommagés à l'avenir.
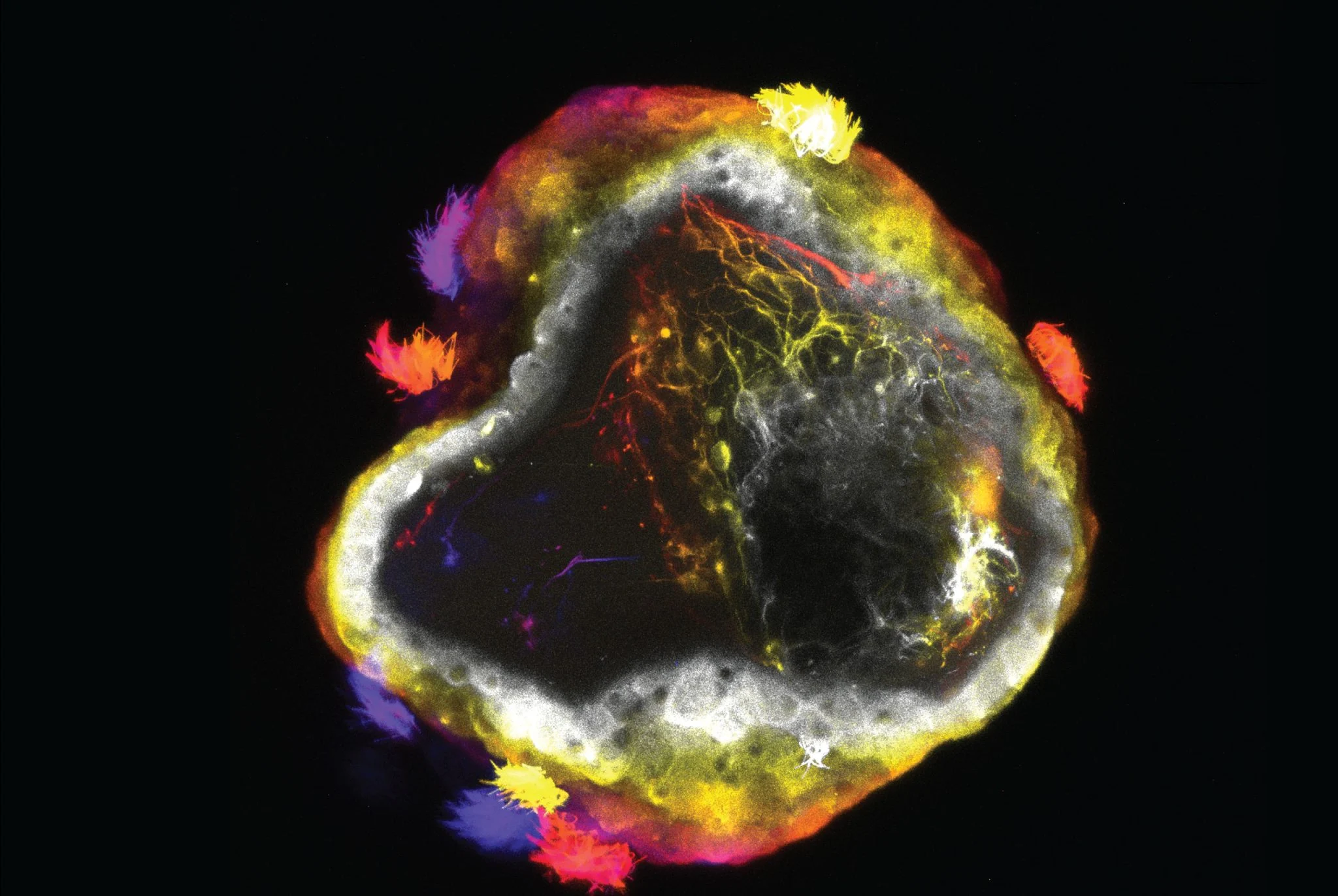
Dans des expériences spécifiques, l’équipe a d’abord isolé des cellules cutanées précurseurs des premiers embryons de Xenopus. Ces cellules se regroupent naturellement en petites structures sphériques dans une boîte de culture et leurs surfaces sont recouvertes de cils denses (cellules multi-ciliées). Le balancement coordonné des cils permet au « robot à cellules de grenouille » original de nager dans l'eau. Après avoir ajouté des cellules précurseurs neurales à cette base, le « neurobot » formé a considérablement modifié sa forme par rapport au passé, devenant globalement plus grand et plus élancé.
L'observation microscopique a montré que ces neurones intégrés développaient non seulement des structures dendritiques et axonales typiques, mais exprimaient également des marqueurs protéiques liés aux synapses, indiquant que les connexions entre les cellules étaient établies et capables de transmettre des signaux. Grâce à la technologie d’imagerie calcique, les chercheurs ont en outre confirmé que les neurones à l’intérieur du neurorobot sont capables d’activité électrique et forment un réseau neuronal fonctionnel simplifié.
L’ajout de systèmes nerveux modifie également considérablement le comportement de ces machines vivantes. Comparés aux robots biologiques sans neurones, les neurorobots ont des activités globales plus fréquentes et des trajectoires de mouvement plus complexes, montrant des schémas de mouvements répétitifs plutôt que de simples lignes droites ou des marches aléatoires. Pour tester le rôle de l'activité neuronale dans le comportement, l'équipe a utilisé le pentylènetétrazole, un médicament connu pour affecter l'activité cérébrale et induire des réponses épileptiformes, et a observé son effet sur le mouvement de ces structures vivantes. Les résultats montrent que le médicament modifie les schémas de mouvement des neurorobots d'une manière complètement différente de celle des machines biologiques qui ne contiennent pas de neurones, ce qui indique que les réseaux neuronaux nouvellement formés façonnent activement le comportement de ces « machines ».
Fotovat a déclaré que ce travail ne consiste pas seulement à ajouter une « unité de contrôle » au robot biologique, mais plus important encore, à inverser les principes internes de la formation du système nerveux. Elle a souligné que, comparés au suivi de la participation des neurones à la production de comportements chez des animaux matures tels que le poisson zèbre, les neurorobots fournissent une plate-forme pour construire des systèmes nerveux « à partir de zéro », de sorte que nous pouvons nous demander : « Mettez les neurones dans une situation totalement sans précédent, selon quelles règles innées vont-ils s'organiser en réseaux ?
Levine a souligné que la neurorobotique offre une opportunité unique d'étudier "comment les réseaux de neurones influencent le mouvement et le comportement dans un système doté d'un corps". Dans les modèles expérimentaux traditionnels, le corps et le système nerveux ont souvent connu une longue histoire de coévolution, tandis que les neurorobots constituent une toute nouvelle combinaison sans contexte évolutif, qui permet d’éliminer les facteurs d’apprentissage et d’évolution et d’observer intuitivement comment les cellules et les réseaux fonctionnent ensemble dans les structures physiques.
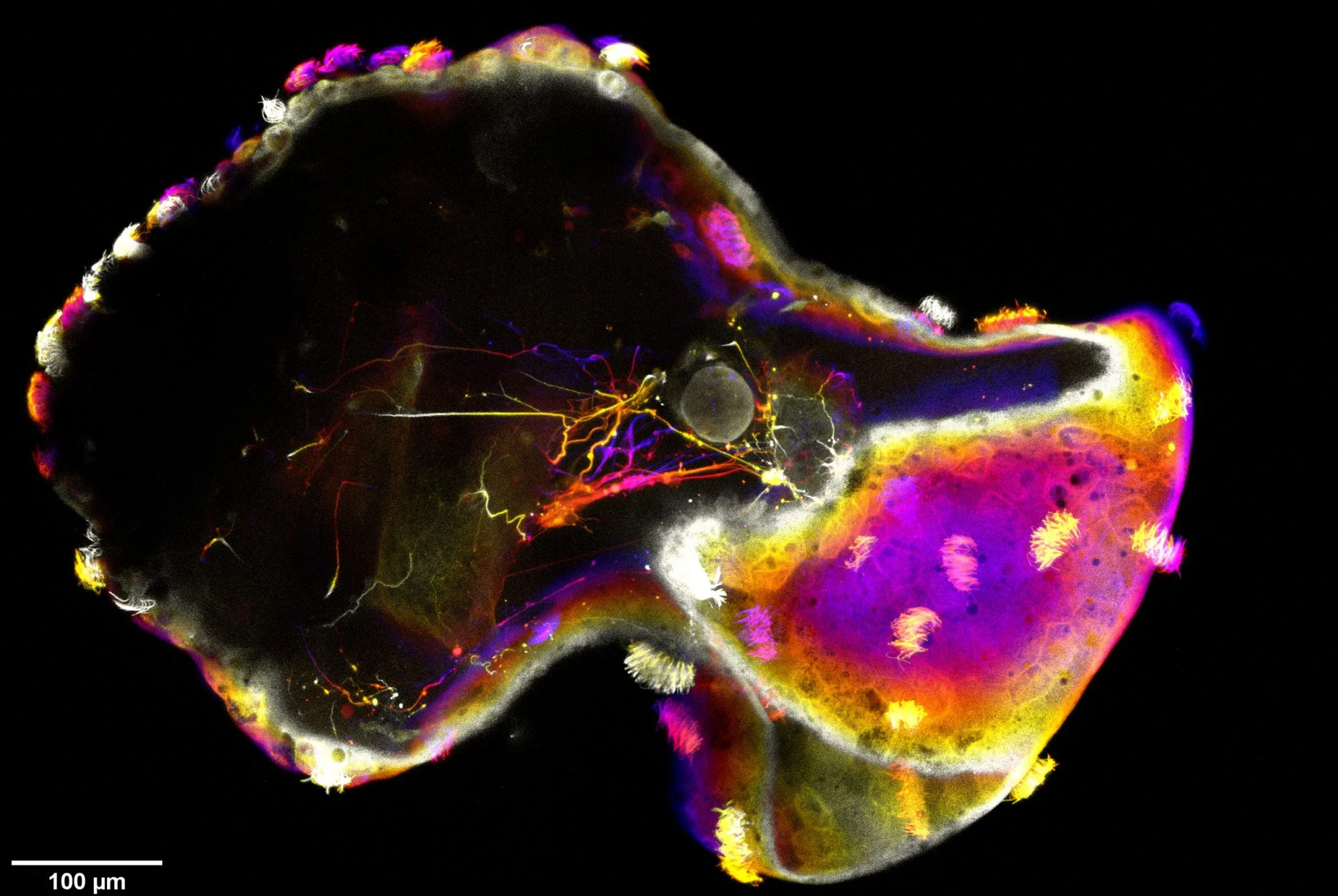
En plus des changements morphologiques et comportementaux, les chercheurs ont également découvert des modèles d’expression génétique inattendus chez les neurobots. En plus des gènes liés aux principaux récepteurs cérébraux, l’équipe a également détecté l’activation d’un certain nombre de gènes impliqués dans le traitement visuel, y compris des gènes normalement exprimés dans les cellules sensibles à la lumière de l’œil. Cela signifie que si leur durée de vie est encore prolongée et que les conditions de culture sont optimisées, les neurorobots pourraient développer la capacité de réagir à la lumière à l’avenir.
Levin a proposé une hypothèse prospective : ces neurorobots pourraient « pré-réguler » certains modules génétiques utiles pour de potentielles fonctions futures en préparation d’une évolution fonctionnelle ultérieure. "S'ils vivent plus longtemps, développeront-ils davantage de véritables photorécepteurs ?" Il a déclaré qu’il s’agissait d’une question que l’équipe explorait actuellement activement.
Les chercheurs ont souligné que pour « construire des choses complètement nouvelles » avec des matériaux biologiques, il faut d'abord comprendre comment les cellules elles-mêmes résolvent les problèmes et prennent des « décisions » dans des environnements inconnus. Les neurorobots constituent précisément une telle plate-forme expérimentale : ils n'ont pas de programmes de développement établis ni de modèles structurels laissés par la sélection naturelle, mais ils montrent néanmoins la capacité de s'auto-organiser, de former des réseaux et de générer des comportements. Cela remet non seulement en question notre compréhension traditionnelle de la frontière entre « corps » et « système nerveux », mais ouvre également l'imagination pour de futurs systèmes vivants programmables, tels que des dispositifs micromédicaux d'auto-guérison et des composants intelligents d'ingénierie tissulaire.